Introducción
El MgSO4 continúa siendo el tratamiento recomendado por la Organización Mundial de la Salud y representa la primera opción terapéutica en las unidades de obstetricia para el manejo de pacientes con preeclampsia y/o eclampsia. A pesar de su uso clínico prolongado, aún no se conoce con exactitud su mecanismo de acción (1-4). Su aplicación se fundamenta en los efectos beneficiosos observados durante su administración, entre los que se incluyen propiedades anticonvulsivantes, antihipertensivas y vasodilatadoras, además de su capacidad para reducir la isquemia cerebral y placentaria, proteger las células endoteliales, disminuir la producción de mediadores inflamatorios y ejercer efectos antioxidantes (5-8).
La preeclampsia se ha asociado con un desarrollo placentario anómalo y disfunción endotelial, caracterizados por un aumento en las citocinas proinflamatorias y un desequilibrio entre la producción de especies reactivas del oxígeno (ROS) y la capacidad antioxidante. Este desequilibrio favorece el estrés oxidativo y la aparición de respuestas inflamatorias que pueden resultar perjudiciales tanto para la madre como para el feto (9-11).
La placenta humana cumple un papel esencial en el desarrollo exitoso del embarazo. Su formación depende de una compleja serie de interacciones entre los componentes maternos y fetales, que permiten establecer la interfase materno fetal, fundamental para el intercambio de nutrientes y oxígeno necesarios durante toda la gestación (9). Sin embargo, sus características únicas dificultan el estudio de su funcionamiento mediante modelos animales. En las últimas décadas, se han desarrollado diversos modelos experimentales para investigar la función placentaria humana, tales como sistemas de perfusión placentaria, cultivos de células aisladas, cultivos primarios de tejido o explantes, análisis histológicos y estudios inmunohistoquímicos (12). Estos enfoques han permitido el estudio de las interacciones celulares y del comportamiento placentario en condiciones fisiológicas y patológicas. En particular, los cultivos de explantes placentarios se han consolidado como una herramienta valiosa, ya que conservan la arquitectura histológica básica de las vellosidades (incluyendo citotrofoblasto, sinciciotrofoblasto, células intersticiales e inmunológicas), lo cual permite simular, en un entorno controlado, las condiciones propias de embarazos normales o patológicos (12,13).
El embarazo es considerado un estado de estrés oxidativo fisiológico. Las ROS desempeñan un papel clave en distintas etapas gestacionales, especialmente en la regulación del flujo sanguíneo útero placentario (11,14-16). Algunos autores describen a la placenta como un órgano rico en mitocondrias, lo cual explica la elevada producción de ROS incluso en embarazos normales (9,14).
A pesar de los avances obtenidos, persisten interrogantes sobre cómo actúa el MgSO4 en la producción o modulación de marcadores de estrés oxidativo en explantes de placenta del tercer trimestre provenientes de embarazos normales, expuestos a condiciones inflamatorias y/o de hipoxia similares a las observadas en la preeclampsia. En este contexto, el presente estudio tiene como objetivo evaluar el efecto del MgSO4 sobre el estrés oxidativo en cultivos de explantes placentarios del tercer trimestre bajo condiciones controladas de inflamación e hipoxia. Los resultados contribuirán a esclarecer los mecanismos de acción de este fármaco sobre el tejido placentario humano.
Materiales y métodos
Recolección de tejidos
Las placentas fueron obtenidas por cesárea o parto vaginal, excluyéndose aquellos casos con inducción del trabajo de parto. De cada placenta se seleccionaron cotiledones sin signos de isquemia, acumulación grasa o necrosis tisular. A cada cotiledón se le removió cuidadosamente la capa decidual y la membrana placentaria, para obtener explantes de la porción media, con un peso húmedo entre 1,5 y 3,0 mg.
Los explantes se cultivaron en placas tipo NUNCTM de 24 pozos (Greiner Bio-One, N° 142475), colocando un solo explante por pozo, en un volumen de 1,5 mL de medio RPMI-1640 (GIBCO BRL, N° 31800- 014), suplementado con: 10% de suero fetal bovino inactivado, 1% de penicilina/estreptomicina, 0,1% de gentamicina, 1% de anfotericina B, 1% de L-glutamina, 1% de aminoácidos no esenciales y 1% de piruvato de sodio.
Durante las primeras 24 horas, se consideró una fase de estabilización, durante la cual el sobrenadante fue descartado, con el objetivo de permitir la adaptación de los tejidos a las condiciones experimentales. Posteriormente, los recambios del medio se realizaron cada 24 horas. Los cultivos se mantuvieron en una incubadora Fisher Scientific a 37 °C, en una atmósfera húmeda compuesta por 5% de CO2, 10% de O2 y balanceada con nitrógeno.
La viabilidad y funcionalidad de los explantes se evaluaron mediante la determinación de la actividad de lactato deshidrogenasa (LDH) y los niveles de gonadotrofina coriónica humana fracción beta (hCG-β), utilizando el método de electroquimioluminiscencia en los sobrenadantes de cultivo (12, 16) (datos no mostrados).
Tras la fase de estabilización, los explantes se dividieron en dos grupos experimentales: uno mantenido en condiciones de normoxia (5% CO2, 10% O2 y nitrógeno), y otro en condiciones de hipoxia (5% CO2, 2–3% O2 y nitrógeno). Ambos grupos fueron incubados durante 24 horas a 37 °C en cámaras húmedas independientes.
Posteriormente, se realizó el recambio por medio fresco y los explantes se asignaron a los siguientes grupos experimentales:
- Grupo control (Medio): mantenido en medio de cultivo base.
- Grupo MgSO4: se adicionó MgSO4 (Sigma-Aldrich, N° M2643) a una concentración final de 2 mM.
- Grupo LPS: se añadió lipopolisacárido de Escherichia coli 055:B5 (LPS; Sigma-Aldrich, N° L2880) a una concentración final de 2 μg/mL [13].
- Grupo MgSO4 / LPS: explantes pretratados con MgSO4, seguidos por la exposición a medio con MgSO4 y LPS.
- Grupo LPS / MgSO4: explantes previamente tratados con LPS durante 24 horas, seguidos por exposición a medio con LPS y MgSO4, manteniendo las concentraciones previamente indicadas.
Determinación de TBARS y NO
Los sobrenadantes de los cultivos se recolectaron diariamente y se centrifugaron a 3.500 rpm durante 15 minutos para eliminar residuos celulares. Posteriormente, fueron almacenados a -20 °C hasta su análisis.
La cuantificación de TBARS se realizó mediante una modificación del método descrito por Feix et al. (17). La medición de los niveles de NO se llevó a cabo utilizando un kit comercial Griess Reagent Kit “for nitrite quantification ” (Molecular Probes , N° G7921), siguiendo las indicaciones técnicas del fabricante. Todas las determinaciones se realizaron por duplicado.
Análisis estadístico
Los datos fueron analizados utilizando el software SPSS versión 10.0 para Windows. Las comparaciones entre condiciones experimentales se realizaron mediante la prueba de Mann-Whitney, considerando diferencias estadísticamente significativas aquellas con p < 0,05. Los resultados se expresan como media ± desviación estándar y n representa el número de placentas incluidas en cada análisis.
Consideraciones bioéticas
Todas las participantes firmaron un consentimiento informado, tras recibir una explicación oral y escrita sobre los objetivos del estudio. El protocolo de investigación fue aprobado por el Comité de Bioética de la Universidad Simón Bolívar y del Hospital Universitario de Caracas, bajo las condiciones descritas, emitiendo un dictamen favorable para la realización del estudio.
Resultados
La Figura 1 muestra las concentraciones de TBARS, expresadas en picomoles de malondialdehído por miligramo de proteína (pmol MDA/mg de proteína), determinadas en los sobrenadantes de los cultivos de explantes de placenta bajo condiciones de normoxia e hipoxia, según los diferentes grupos experimentales. Se observa que los niveles de TBARS fueron consistentemente más bajos en condiciones de normoxia que en hipoxia, mostrando diferencias estadísticamente significativas en cada comparación (*p < 0,01; ***p < 0,03).
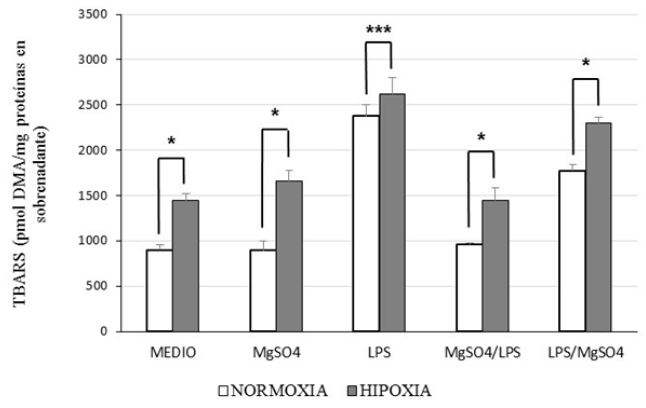
Figura 1. Concentración de TBARS (pmol de malondialdehído/mg de proteína) en sobrenadantes de explantes placentarios cultivados por 72 horas bajo condiciones de normoxia e hipoxia. Se evaluaron cinco grupos experimentales: medio basal (Medio), MgSO4 (2 mM), LPS (2 μg/mL), pretratamiento con MgSO4 seguido de LPS (MgSO4/LPS), y tratamiento inverso (LPS/MgSO4). Los valores se expresan como media ± desviación estándar (n=7). Comparaciones estadísticas realizadas mediante prueba de Mann- Whitney (*p<0,01; ***p<0,03).
Tanto en normoxia como en hipoxia, los niveles de TBARS se incrementaron de manera significativa en los cultivos tratados con LPS en comparación con los demás grupos. Además, en condiciones hipóxicas, se observó un aumento adicional de TBARS en los cultivos que fueron tratados con MgSO4 seguido de LPS, así como en aquellos que recibieron LPS antes de la administración de MgSO4, con diferencias significativas en ambos casos (*p < 0,01).
Al comparar los tratamientos bajo normoxia, no se observaron diferencias estadísticamente significativas entre los cultivos con medio base, aquellos tratados solo con MgSO4 y los pretratados con MgSO4 antes de la exposición a LPS. Por otro lado, en hipoxia, no hubo diferencias significativas entre los cultivos con medio base y los pretratados con MgSO4 antes de la exposición a LPS.
En la Figura 2, se presentan los niveles NO, expresados en micromoles (μM), determinados en los sobrenadantes de los cultivos de explantes bajo condiciones de normoxia e hipoxia para cada uno de los tratamientos.
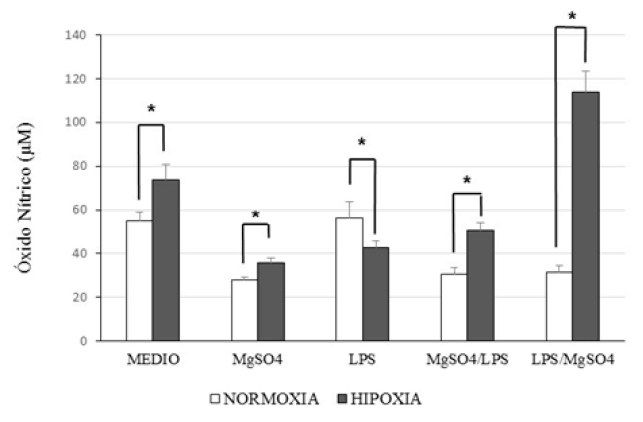
Figura 2. Concentración de óxido nítrico (μM) en sobrenadantes de explantes placentarios cultivados durante 72 horas bajo condiciones de normoxia e hipoxia. Se analizaron los siguientes grupos: medio basal (Medio), MgSO4 (2 mM), LPS (2 μg/mL), tratamiento combinado MgSO4/LPS y LPS/MgSO4. Los valores se presentan como media ± desviación estándar (n=7). Las diferencias estadísticas se determinaron mediante prueba de Mann-Whitney (*p<0.01 y ***p<0.03).
En condiciones de normoxia, los cultivos tratados únicamente con medio base o con MgSO4 mostraron niveles más bajos de NO en comparación con los mismos tratamientos en condiciones hipóxicas, con diferencias estadísticamente significativas (*p < 0,01). Asimismo, los cultivos tratados con LPS en normoxia presentaron niveles de NO más altos que aquellos en hipoxia, también con significancia estadística (*p < 0,01).
En los grupos tratados con MgSO4 seguido de LPS, y viceversa, los niveles de NO fueron significativamente más bajos bajo normoxia en comparación con los valores observados en hipoxia (*p < 0,01).
El análisis de medias y desviaciones estándar de las concentraciones de NO mostró que, bajo normoxia, no hubo diferencias significativas entre los cultivos con medio base y los tratados con LPS, ni entre aquellos tratados con MgSO4 y los tratados primero con MgSO4 y luego con LPS. En cambio, bajo condiciones de hipoxia, todas las comparaciones entre tratamientos arrojaron diferencias estadísticamente significativas.
Discusión y conclusiones
La placenta humana se desarrolla inicialmente en condiciones de baja oxigenación (~1–3%), las cuales son esenciales para la invasión y diferenciación celular del trofoblasto en citotrofoblasto. Este proceso facilita la remodelación de las arteriolas espirales del endometrio y la formación del sinciciotrofoblasto. Tras el establecimiento de la circulación útero placentaria (alrededor de la semana 12) la tensión de oxígeno se incrementa progresivamente hasta alcanzar niveles más cercanos a los de la sangre materna (~8–12%), manteniéndose así durante el resto del embarazo (10,12,18-20).
Estudios previos, como los realizados por Genbacev et al . (1996) (21), demostraron que la hipoxia favorece la invasión del citotrofoblasto durante el primer trimestre, mientras que en etapas más avanzadas del embarazo este entorno estimula la diferenciación hacia sinciciotrofoblasto. En cultivos de explantes placentarios a término, condiciones hipóxicas inducen la liberación de factores solubles que afectan el metabolismo celular, la viabilidad, la angiogénesis y la integridad mitocondrial, e incluso contribuyen a la muerte celular endotelial (22).
Con el objetivo de simular las condiciones placentarias tanto fisiológicas como patológicas, se diseñó un modelo experimental que reproducía tensiones de oxígeno observadas en embarazos normales (~10%) y en preeclampsia (~3%) (12,18,19,23-25). Esta estrategia permitió reproducir in vitro los cambios fisiológicos y bioquímicos propios de la disfunción placentaria. Al tratar los explantes con MgSO4, antes y después de la exposición a LPS en ambos escenarios de oxigenación, se logró evidenciar su efecto modulador sobre marcadores de estrés oxidativo. La aplicación simultánea de los tratamientos permitió, además, comparar la respuesta del tejido ante el fármaco en ambientes normóxicos e hipóxicos, ofreciendo una perspectiva más completa sobre su mecanismo de acción y un modelo experimental confiable para futuras investigaciones (1,19,26-29).
Aunque se utilizó una concentración de 2 mM de MgSO4 en los cultivos, diversos estudios han reportado que concentraciones séricas terapéuticas en gestantes con preeclampsia alcanzan entre 3 y 4 mM (3,30). En este contexto, sería relevante explorar si concentraciones superiores podrían potenciar el efecto antioxidante del MgSO4 bajo condiciones de hipoxia, sin inducir apoptosis. Estudios previos han demostrado que 4 mM de MgSO4 pueden revertir la peroxidación lipídica y restaurar la actividad de la Ca2+-ATPasa en membranas placentarias [30], lo que sugiere que futuras investigaciones deberían considerar un rango más amplio de dosis para evaluar su eficacia y seguridad.
Los resultados obtenidos revelan que el tratamiento con MgSO4 posterior a la exposición inflamatoria inducida por LPS ocasiona una disminución significativa en los niveles de TBARS, tanto bajo normoxia como hipoxia. Este hallazgo coincide con estudios previos en los que se evidenció que el LPS incrementa el estrés oxidativo en cultivos de explantes placentarios (31), mientras que el MgSO4 reduce la peroxidación lipídica y estabiliza membranas celulares, favoreciendo la actividad de bombas como la Ca2+-ATPasa (32,33).
La acción antioxidante del MgSO4 parece estar mediada por su capacidad para bloquear la interacción del Ca2+ con los fosfolípidos de membrana, lo que previene la exposición de cadenas hidrocarbonadas a los radicales libres (7, 33). Así, el mantenimiento de la homeostasis de Mg2+ en el tejido placentario emerge como un factor crucial para un desarrollo gestacional saludable (7).
Por otro lado, los niveles de NO se comportaron de manera diferencial según las condiciones de oxigenación. En presencia de LPS, los cultivos mostraron un aumento de NO en condiciones de hipoxia, probablemente por activación de macrófagos vía IFN-γ y expresión inducible de la enzima iNOS (34-36). Sin embargo, en la mayoría de los tratamientos (excepto aquellos con hipoxia severa), el MgSO4 se asoció con una reducción en la producción de NO, lo que refuerza su rol modulador del estrés nitrógeno específico.
Se ha demostrado que la NOS presente en macrófagos es inducible. Los macrófagos no estimulados no tienen la enzima, pero la activación de estas células se acompaña de la aparición irreversible de la enzima iNOS. Blanchette et al., (2003), evaluaron la participación de diferentes segundos mensajeros, en la regulación de la producción de NO estimulada por IFN-g en macrófagos. Estos investigadores observaron que todos los efectos de reducción en la regulación en la producción de iNOS se produjeron a nivel pretranscripcional, a excepción de NFkB, que parece ejercer su papel en la producción de NO a través de un evento iNOS-independiente. Además, observaron que el mensajero STAT1α es esencial para la expresión de iNOS inducido por el IFN-g en los macrófagos y por ende en la producción de NO, mientras que la contribución de NFkB a esta regulación celular parece ser mínima (35).
En la preeclampsia, la remodelación deficiente de las arteriolas espirales durante el inicio del embarazo favorece una isquemia placentaria. Esta condición incrementa el estrés oxidativo (incremento en la peroxidación lipídica, especies reactivas al oxígeno y especies reactivas al nitrógeno), además de presentarse una disminución en la capacidad antioxidante por parte del tejido placentario, por disminución de la SOD (superóxido dismutasa), GPx (glutatión peroxidasa) y CAT (Catalasa). Simultáneamente, el incremento de los niveles de estrés oxidativo en la placenta durante esta patología, beneficia la producción de citocinas proinflamatorias con la inadecuada producción de citocinas antinflamatoria (36). Además, el establecimiento de la isquemia placentaria, permite que los factores antiangiogénicos como el sFLT-1 (soluble fms-like tyrosine kinase 1) aumenten en circulación, permitiendo que todos estos factores contribuyan al establecimiento de un cuadro de disfunción vascular generalizado (20). Sin embargo, diversos estudios han permitido conocer como la administración de MgSO4 permite generar una disminución de los niveles de sFLT-1 y endoglobina, así como bloquear los receptores de NMDA (N-metyl-D-aspartate) a nivel cerebral, disminuir la producción de citocinas inflamatorias, así como la activación de la sintetasa de NO , bloqueo de arginasas y reducción de los radicales libres (37).
Estos hallazgos sugieren que el MgSO4 podría modular diversas vías celulares, tanto antioxidantes como inflamatorias, al interferir en cascadas activadas por citocinas proinflamatorias, especies reactivas y factores antiangiogénicos como sFLT-1 (36-37).
Los resultados obtenidos consolidan el papel del MgSO4 como modulador del estrés oxidativo en condiciones inflamatorias y de hipoxia, simuladas mediante explantes placentarios humanos. Su aplicación previa al estímulo patológico mostró ser más efectiva, reduciendo significativamente los niveles de TBARS y NO , lo que sugiere un mecanismo preventivo y estabilizador de membranas celulares.
Estos efectos podrían explicarse por la interferencia del MgSO4 en procesos dependientes del calcio intracelular, como la activación de enzimas oxidativas y la desestabilización de fosfolípidos de membrana. Asimismo, la modulación de la actividad de la Ca2+- ATPasa y la posible reducción de mediadores como sFlt-1 refuerzan su potencial terapéutico en escenarios de disfunción placentaria.
Dado que el estrés oxidativo está implicado en múltiples complicaciones gestacionales (entre ellas la preeclampsia), estos hallazgos abren nuevas vías para explorar el MgSO4 como agente adyuvante en intervenciones clínicas dirigidas al tejido placentario.
El modelo experimental empleado, al reproducir ambientes fisiológicos y patológicos en paralelo, constituye una plataforma útil para seguir investigando los mecanismos moleculares y bioquímicos que subyacen a su acción. Futuras investigaciones podrían centrarse en caracterizar los receptores específicos, las vías de señalización implicadas y el impacto del MgSO4 en otros tipos celulares presentes en la placenta, incluyendo inmunomoduladores, angiogénicos y antioxidantes.
Declaración financiamiento y conflictos de interés
Este trabajo fue parcialmente apoyado por la subvención PG 09-6579-2006 de CDCH-UCV y por una subvención de Decanato de Postgrado USB. Los autores reportan ningún conflicto de intereses. Los autores solo son responsables del contenido y la redacción del documento.
Contribuciones de autores
- Concepción y diseño de los experimentos: JMG, MIC, YCC.
- Realizó los experimentos: JMG, MIC.
- Análisis e interpreetación de datos: JMG, MIC.
- Redacción del manuscrito: JMG, YCC.
- Revisión del manuscrito: JMG, YCC
Referencias
- Euser AG, Cipolla MJ. Magnesium sulfate treatment for the prevention of eclampsia: A brief review. NIH Public Access. 2009;1169-1175. https://doi.org/10.1161/STROKEAHA.108.527788
- Organización Mundial de la Salud. Recomendaciones de la OMS para la prevención y el tratamiento de la preeclampsia y la eclampsia [Internet]. 2011. [citado 29 Jun 2025]. Disponible en: https://www.who.int/es/publications/i/item/9789241548335
- Abad C, Vargas F, Zoltan T, Proverbio T, Piñero S, Proverbio F, et al . Magnesium sulfate affords protection against oxidative damage during severe preeclampsia. Placenta 2015;36(2):179-185. https://doi.org/10.1016/j.placenta.2014.11.008
- Benites-Cóndor Y, Bazán-Ruiz S, Valladares-Garrido D. Factores asociados al desarrollo de preeclampsia en un Hospital de Pirua, Perú. CIMEL 2011;16(2):77- 82. [citado 29 Jun 2025]. Disponible en: https://www.redalyc.org/pdf/717/71723601003.pdf
- Holcberg G, Amash A, Sapir O, Hallak M, Sheiner E, Ducler D, et al . Different effects of magnesium sulfate and angiotensin II on the capacity of the fetal and maternal compartments of normal human placenta to secrete TNF-a and IL-6. J Reprod Immunol 2006;69(2):115- 125. https://doi.org/10.1016/j.jri.2005.09.005
- Kao M-C, Jan W-C, Tsai P-S, Wang T-Y, Huang C-J. Magnesium Sulfate Mitigates Lung Injury Induced by Bilateral Lower Limb Ischemia-Reperfusion in Rats. J Surg Res 2011;171(1):e97-e106. https://doi.org/10.1016/j.jss.2011.03.028
- Chiarello D, Marin R, Proverbio F, Coronado P, Fernando T, Salsoso R, et al . Mechanisms of the effect of magnesium salts in preeclampsia. Placenta 2018;69:134- 139. https://doi.org/10.1016/j.placenta.2018.04.011
- Shahi A, Aslani S, Ataollahi M, Mahmoudi M. The role of magnesium in different inflammatory diseases. Inflammopharmacology 2019;27(4):649-661. https://doi.org/10.1007/s10787-019-00603-7
- Chaddha V, Viero S, Huppertz B, Kingdom J. Developmental biology of the placenta and the origins of placental insufficiency. Semin Fetal Neonatal Med 2004;9(5):357-369. https://doi.org/10.1016/j.siny.2004.03.006
- Corría J, Cruz Manzano E. Balance entre las especies reactivas y los sistemas antioxidantes en la gestación normal. Rev Cubana Obstet Ginecol 2009;35(2). http://scielo.sld.cu/pdf/gin/v35n2/gin05209.pdf
- Camacho Terceros LA, Berzaín Rodríguez MC. Revisión- Una mirada clínica al diagnóstico de preeclampsia. Rev Cient Cienc Méd 2015;18(1):50-55. http://www.scielo.org.bo/scielo.php?script=sci_arttext&pid=S1817-74332015000100010&lng=es
- Miller RK, Genbacev O, Turner MA, Aplin D, Caniggia I, Huppertz B. Human Placental Explants in Culture: Approaches and Assessments. Placenta 2005;26(3):439-448. https://doi.org/10.1016/j.placenta.2004.10.002
- Faye A, Pornprasert S, Dolcini G, Ave P, Taïeb J, Taupin JL, et al . Evaluation of the placental environment with a new in vitro Model of histocultures of early and term placentae: Determination of cytokine and chemokine expression profiles. Placenta 2005;26(2-3):262-267. https://doi.org/10.1016/j.placenta.2004.08.005
- Núñez-González J, Sanabria-Vera C, Romero- Adrián T, Núñez L, Montiel I, Boscán F, et al . Óxido nítrico, malondialdehído, perfil lipídico, factor de necrosis tumoral alfa y sus receptores solubles en mujeres no embarazadas, gestantes normales y preeclámpticas. Gac Med Caracas 2001;109(3):352- 360. [citado 29 Jun 2025]. Disponible en: http://ve.scielo.org/scielo.php?script=sci_arttext&pid=S0367-47622001000300008&lng=es
- Li-Tung H, Chih-Sung H, Kow-Aung C, You-Lin T. Roles of nitric oxide and asymmetric dimethylarginine in pregnancy and fetal programming. Int J Mol Sci 2012;13(11):14606-14622. https://doi.org/10.3390/ijms131114606
- Goncalves JM, Camejo MI, Casart Y. Nitric oxide and oxidative stress in placental explant cultures. Syst Biol Reprod Med 2016;62(1):11-16. https://doi.org/10.3109/19396368.2015.1075163
- Feix J, Bachowski G, Girotti A. Photodynamic action of merocyanine 540 on erythocyte membranes: structural perturbation of lipid and protein contituents. Biochim Biophys Acta. 1991;1075(1):28-35. https://doi.org/10.1016/0304-4165(91)90070-w
- Sullivan M, Galea P, Latif S. What is the appropriate oxygen tension for in vitro culture? Letter to the Editor. Mol Hum Reprod 2006;12(11):653. https://doi.org/10.1093/molehr/gal081
- Tuuli MG, Longtine MS, Nelson DM. Review: Oxygen and trophoblast biology- A source of controversy. Placenta 2011;32(Suppl 2):S109-S118. https://doi.org/10.1016/j.placenta.2010.12.013
- Chiarello D, Abad C, Rojas D, Toledo F, Vásquez CM, Mate A, et al . Oxidative stress: Normal pregnancy versus preeclampsia. BBA-Mol Basis Dis 2020;1866(2):165354. https://doi.org/10.1016/j.bbadis.2018.12.005
- Genbacev O, Joslin R, Damsky CH, Polliotti BM, Fisher SJ. Hypoxia Alters Early Gestation Human Cytotrophoblast Differentiation/Invasion. In Vitro and Models the Placental Defects that Occur in Preeclampsia. J Clin Invest 1996;97(2):540-550. https://doi.org/10.1172/JCI118447
- Robinson NJ, Wareing M, Hudson NK, Blankley RT, Baker PN, Aplin JD, et al . Oxygen and the liberation of placental factors responsible for vascular compromise. Lab Invest 2008;88(3):293-305. https://doi.org/10.1038/labinvest.3700746
- Gude NM, Stevenson JL, Moses EK, King R. Magnesium regulates Hypoxia- stimulated apoptosis in the human placenta. Clin Sci 2000;98(4):375-380. [citado 29 Jun 2025]. Disponible en: https://pubmed.ncbi.nlm.nih.gov/10731470/
- Nevo O, Soleymanlou N, Wu Y, Xu J, Kingdom J, Many A, et al . Increased expression of sFlt-1 in in vivo and in vitro models of human placental hypoxia is mediated by HIF-1. Am J Physiol Regul Integr Comp Physiol 2006;291(4):R1085-R1093. https://doi.org/10.1152/ajpregu.00794.2005
- Reti NG, Lappas M, Huppertz B, Riley C, Woldek ME, Henschke P, et al . Effect of high oxygen on placental function in short-term explant cultures. Cell Tissue Res 2007;328(3):607-616. https://doi.org/10.1007/s00441 006-0375-1
- Cnossen JS, Ter Riet G, Mol BW, Van Der Post JA, Leeflang MM, Meads CA, et al . Are tests for predicting pre-eclampsia good enough to make screening viable? A review of reviews and critical appraisal of eclampsia and imminent. Acta Obstet Gynecol 2009;88(7):758- 765. https://doi.org/10.1080/00016340903008953
- Duley L, Gülmezoglu M, Henderson-Smart DJ, Chou D. Magnesium sulphate and other anticonvulsants for women with pre-eclampsia. Cochrane Database Syst Rev [Internet]. 2010;2010(11):CD000025. https://doi.org/10.1002/14651858.CD000025.pub2
- Reyna-Villasmil E, Briceño-Perez C, Torres-Cepeda D. Marcadores bioquímicos para la predicción de la preeclampsia. Rev Obstet Ginecol Venez 2010;70(1):53- 66. [citado 29 Jun 2025]. Disponible en: https://ve.scielo.org/scielo.php?script=sci_arttext&pid=S0048-77322010000100010
- Turner JA. Diagnosis and management of pre-eclampsia an update. Int J Womens Health 2010;(2):327-337. https://doi.org/10.2147/IJWH.S8550R
- Marín R, Abad C, Rojas D, Fernández M, Ruette F. Magnesium sulfate in oxidative stress-associated pathologies: clinical, cellular, and molecular perspectives. Biophys Rev 2025;17(2):511-535. https://doi.org/10.1007/s12551-025-01292-z
- Malek A, Sager R, Schneider H. Pathobiology: Oxidant Stress, Angiogenesis and Neoplasia. Placenta. 2001;22(Suppl. A):S45-S50. https://doi.org/10.1053/plac.2001.0635
- Abad C, Teppa-Garrán A, Proverbio T, Piñero S, Proverbio F, Marín R. Effect of magnesium sulfate on the calcium-stimulated adenosine triphosphatase activity and lipid peroxidation of red plblood cell membranes from preeclamptic women. Biochem Pharmacol 2005;70(11):1634-1641. https://doi.org/10.1016/j.bcp.2005.09.009
- Chiarello DI, Marín R, Proverbio F, Benzo Z, Piñero S, Botana D, et al . Effect of hipoxia on the calcium and magnesium content, lipid peroxidation level, and Ca2+-ATPase activity of syncytiotrophoblast plasma membranes from placental explants. Bio Med Res Int 2014;2014:597357
- Goldsby RA, Kindt TJ, Osborne BA, Kuby J. Inmunología. 5a ed. México, D.F.: McGraw-Hill Interamericana; 2004. 700 p
- Blanchette J, Jaramillo M, Olivier M. Signalling events involved in interferon-gamma-inducible macrophage nitric oxide generation. Immunology. 2003;108(4):513- 522. https://doi.org/10.1046/j.1365-2567.2003.01620.x
- Goncalves JM, Casart YC, Camejo MI. Sulfato de Magnesio y su acción anti-inflamatoria en explantes de placenta. Acta Cient Soc Venez Bioan Esp 2019;22(2):37-47. [citado 29 Jun 2025]. Dissponible en: https://saber.ucv.ve/ojs/index.php/rev_ACSVBE/article/view/21455
- Hannan NJ, Brownfoot FC, Cannon P, Deo M, Beard S, Nguyen TV, et al . Resveratrol inhibits release of soluble fms-like tyrosine kinase (sFlt-1) and soluble endoglin and improves vascular dysfunction– implications as a preeclampsia treatment. Scientific Rep 2017;7(1):1819. https://doi.org/10.1038/s41598-017-01993-w
